(関連目次)→妊娠したら気をつけること 目次 産科一般
ぽち→ 
(投稿:by 僻地の産科医)
トキソプラズマという病気は、
あまり皆さんになじみのない病気だと思います。
ですが、この病気。妊娠初期にかかると
大変な奇形を胎児に引き起こすので有名な疾患です。
で、妊娠初期に罹っているかどうか調べる施設が多いのは
割と一般的ではないかなと思うのですが、
最近、トキソプラズマ(+)の妊婦さんがいて
調べる機会がありました。
トキソプラズマIgM(+)の患者さんがいて、
産婦人科産科編のガイドラインを見ると、
トキソプラズマIgMは3年くらい陽性である可能性があると。
ここに突如としてIgGアビディティなる言葉が
出てくるのですが、説明が全然わかんない!!!!
という訳でネットで探したけれど、
感染症のスクリーニングとその取り扱い
http://www.jsog.or.jp/PDF/59/5909-382.pdf
結論としてはわかったようなわからんような…
ということで調べてみましたo(^-^)o..。*♡
産科と婦人科の母子感染のところにのってました。(表4が大事)
(図2-4は省略させていただきました)
母子感染 トキソプラズマ
三井記念病院産婦人科
小島俊行 ・菅野素子 ・中尾美木 ・中林 稔 ・中山裕敏、
北條 智 ・柿木成子 ・中田真木 ・安田 孝
(産科と婦人科・第75巻(328)11号 p1662-1672)
妊婦健診のスクリーニング項目にトキソプラズマ抗体検査を追加する施設が増加しているが,その判断に苦慮することがある.妊婦がトキソプラズマIgM抗体陽性であれば,妊娠中の初感染の可能性が生じ,先天感染の可能性も生じる.この場合,妊婦の問診,トキソプラズマIgM抗体の推移,可能であればアビディティの測定を行い感染時期を推定する.ハイリスクであれば,薬物療法を行うか,羊水穿刺による遺伝子診断を行う.ローリスクであれば無治療である.
出生時に膀帯血で検査し,さらにトキソプラズマ抗体の推移を1歳まで行う.
1985年旧厚生省の研究班から,日本には先天性トキソプラズマ症はほとんどみられないと新聞発表されたため,ほとんどの産婦人科医は妊婦健診の感染症スクリーニング項目からトキソプラズマ抗体検査を削除した.ところが1990年代になると,新生児科領域から先天性トキソプラズマ症児の出生の報告が相次ぎ,2000年前後から再び妊婦健診のスクリーニング項目にトキソプラズマ抗体検査が追加され始めた.それでも,トキソプラズマIgM抗体陽性妊婦は先天感染の可能性が否定できず,中絶を余儀なくされることも多かった.しかし現在われわれが行っているトキソプラズマIgG抗体のアビディティ(avidity,抗原結合力)の測定により,600例の妊婦さんのほとんどが中絶を回避し,これまで先天感染のない児を出生している.
概念
トキソプラズマ症(toxoplasmosis)は,胞子虫類に属する細胞内寄生性の病原性原虫であるToxoplasma gondiiにより引き起こされ,典型的な人獣共通感染症(zoonosis)の一種である.
トキソプラズマは,ほとんどすべての陸棲温血脊椎動物(哺乳類,鳥類),一部の爬虫類に感染する.トキソプラズマは宿主細胞に侵入する際,特異レセプターを必要としないため,あらゆる細胞に侵入できる。自然感染経路はオーシストかシスト(嚢胞)による経口感染で,消化酵素によって外殻が壊れ中の原虫(スポロゾイトあるいはブラディゾイト)は小腸粘膜上皮から侵入しそこで増殖しタキゾイトとなる.さらに初期は細胞内のまま血行性およびリンパ行性に,肝・脾・肺さらに全身の各臓器・リンパ器官に播種する.しかし宿主の免疫反応によりタキゾイトの増殖と播種は停止し嚢胞(tissuecyst)を形成する.嚢胞は抗生物質が無効のため,慢性期には,脳・骨格筋・心筋などに嚢胞として永久的に存在する.急性感染を起こした妊婦では寄生虫血症が生じ,タキゾイトが胎盤(絨毛)に感染し増殖し胎児に感染が成立する.すなわち妊娠中に初感染すると,胎内感染により先天感染を生じることがある。
疫学
トキソプラズマは,全人類の10~80%が感染しているといわれている.妊婦の抗体陽性率は,フランス(80%),中央ヨーロッパ(ドイツ(40~50%),スイス(40%),オランダ(40%),ベルギー(50%),デンマーク(30%)),中央アフリカ(50~80%),南米(ブラジル(3(隅))で高く,北米(3~30%),日本(東京近郊7.1%,南九州15%),東南アジア(10%以下)などで低い1-5).
これらの抗体陽性率の差は,食肉習慣の相違(ヨーロッパ,ブラジル,アジア),ネコの抗体保有率の相違(ミクロネシア,エルサルバドル),衛生状態の相違(ブラジル)などが,複雑に関連していると考えられる.
わが国での野良猫の数の指標として,飼い主からの猫引き取り頭数をみると,昭和58年度の約21,000頭をピークに急激に減少し,その後約15年間で1/11以下にまで減少している(東京都動物保護管理審議会,平成11年3月報告).
また,ブタのトキソプラズマ病の発生数の推移をみると,平成元年より激減している。これらの衛生環境の改善の影響か,1967年7月~1970年7月の妊婦のトキソプラズマ赤血球凝集反応(医科研法)陽性率は20.15%(1114/5527)6),1977年の東大分院のトキソプラズマIgG抗体(トキソIgG-EIA「生研」)陽性率は31.8%(27/85)であったが,同じ東京近郊では最近トキソプラズマIgG抗体(トキソIgG-EIA「生研」)陽性率は7.1%(19/266)と低下している.
感染経路
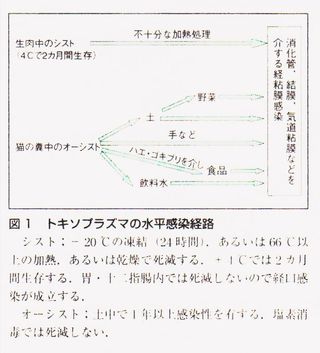
 現在までに報告されているヒトの感染経路として垂直感染と水平感染とがある(表1).経母乳感染は,動物では確認されているが,ヒトでは現在まで確認されていない.水平感染には,主に経粘膜感染(消化管,結膜,気道粘膜〉と血液媒介感染とがある.経口感染の感染源は,ネコの糞に多量に含まれるオーシスト(土,飲料水,ハエ,ゴキブリなど)あるいは食用肉・内臓に含まれるシスト(加熱処理の不十分な肉,生ハム,サラミソーセージ,レバーなど)がある(図1).1995年3月にカナダで急性トキソプラズマ症の集団発生(outbreak)が起こったが,その感染源が市営の水道水であることが報告されたこともある7).
現在までに報告されているヒトの感染経路として垂直感染と水平感染とがある(表1).経母乳感染は,動物では確認されているが,ヒトでは現在まで確認されていない.水平感染には,主に経粘膜感染(消化管,結膜,気道粘膜〉と血液媒介感染とがある.経口感染の感染源は,ネコの糞に多量に含まれるオーシスト(土,飲料水,ハエ,ゴキブリなど)あるいは食用肉・内臓に含まれるシスト(加熱処理の不十分な肉,生ハム,サラミソーセージ,レバーなど)がある(図1).1995年3月にカナダで急性トキソプラズマ症の集団発生(outbreak)が起こったが,その感染源が市営の水道水であることが報告されたこともある7).
母子の感染症状
 妊婦の初感染の症状は,疼痛・化膿傾向を伴わないリンパ腺腫脹(頸部,後頭部,鎖骨窩,腋下,鼠径部),倦怠感,筋肉痛を伴う発熱などである.発疹はまれで,脈絡網膜炎が,急性後天性感染でみられることはまれであるが,おこれば劇的となる.トキソプラズマIgM抗体陽性妊婦のうちこれらの症状を有している妊婦は約6%であった8).図2に,頸部リンパ節腫脹を認めた造影CT写真を示す.図3は,その部の吸引細胞診を示した.中央部に認められる緑色の細胞質を有する細胞の集籏が認められ,これが類上皮細胞肉芽腫に相当するものであり,トキソプラズマ性リンパ節炎と診断された.
妊婦の初感染の症状は,疼痛・化膿傾向を伴わないリンパ腺腫脹(頸部,後頭部,鎖骨窩,腋下,鼠径部),倦怠感,筋肉痛を伴う発熱などである.発疹はまれで,脈絡網膜炎が,急性後天性感染でみられることはまれであるが,おこれば劇的となる.トキソプラズマIgM抗体陽性妊婦のうちこれらの症状を有している妊婦は約6%であった8).図2に,頸部リンパ節腫脹を認めた造影CT写真を示す.図3は,その部の吸引細胞診を示した.中央部に認められる緑色の細胞質を有する細胞の集籏が認められ,これが類上皮細胞肉芽腫に相当するものであり,トキソプラズマ性リンパ節炎と診断された.
先天性トキソプラズマ症の症状は,水頭症,脈絡網膜炎,頭蓋内石灰化,子宮内胎児発育遅延などである.感染時期の診断目的で当科に紹介され,慢性感染と診断されたトキソプラズマIgM抗体陽性妊婦の8歳の第一子は,母親が妊娠中トキソプラズマ抗体検査を受けておらず,念のため第一子のトキソプラズマ抗体を検査し陽性と判明した.さらに,眼底検査を施行したところ(図4),左眼に白色の癩痕性網膜炎を認め,先天性トキソプラズマ症と初めて診断された、現在,トキソプラズマIgM抗体陽性妊婦の既に出生している児100例中10例(10%)に先天感染を認めており,妊婦スクリーニングを行わない場合は非常にハイリスクである.したがって,母体の感染時期によっては,すでに出生している同胞の先天感染の除外が必要である.
トキソプラズマ1gM抗体陽性
妊婦の感染リスク因子
205例のトキソプラズマIgG抗体陰性妊婦と181例のトキソプラズマIgM抗体陽性妊婦について,妊娠前も含め自宅での猫の飼育歴と,生肉の摂取習慣の有無と,ガーデニング・家庭菜園などの土いじり習慣の有無を問診した9).生肉とは,馬田,墨刺,レバ刺,鳥刺,レアステーキ,その他(鹿卜,熊刺など)あるいは,加熱処理の不十分な肉のことである.トキソプラズマIgM抗体陽性妊婦と対照妊婦の猫飼育歴は,各々392%,31.7%に認め有意差を認めなかった(、ρ=0.155).これは,猫の飼育が妊婦のトキソプラズマ急性感染とは相関しないことを示している.通常,ネコが初感染した場合,糞中にトキソプラズマを排出するのは,1~3週間のみであるが,土中でオーシストとなれば,1年間の感染性を有するようになることから土のほうが感染する機会が多いと説明できる.生肉摂取習慣は,各々78.8%,34.6%に認め有意に(p〈0.0001)トキソプラズマIgM抗体陽性妊婦で高値であった.土いじり習慣も,各々47.3%,28.2%に認め,有意に(p=0.0078)トキソプラズマIgM抗体陽性妊婦で高値であった.Cook AJCら10)は,ヨーロッパでトキソプラズマ急性感染の妊婦とトキソプラズマ抗体陰性妊婦とを比較検討した.妊婦の急性感染を最も強力に推定する危険因子は,
①不十分な加熱処理の子羊肉,牛肉,狩猟による鳥獣肉の摂取
②土との接触
③ヨーロッパ外部の国,アメリカ,カナダへの旅行であった.
猫との接触は危険因子ではなかった.著者らの成績もこれと一致した.
妊婦では,加熱処理の不十分な肉の摂取を控え,土いじり後には十分手を洗う必要がある.したがって表2に示すハイリスク妊婦に対しては,トキソプラズマ抗体の測定を行っている.

妊婦の問診項目
一般にトキソプラズマの母子感染が生じるのは,妊婦の初感染の時である.したがって妊婦の感染が疑われる場合,最も重要なことはその感染時期の推定である.表3に問診項目を示した.重要な点は,これらの項目が妊娠前からあれば,妊娠前の初感染の可能性が高くなり先天感染のリスクは低くなるが,妊娠後から始めたのであれば,妊娠後の初感染の可能性が生じ先天感染のリスクは高くなる.すなわち,あるリスク因子の妊娠前の曝露量あるいは曝露期間と妊娠後の曝露量あるいは曝露期間との比率が推定できれば,そのリスク因子による妊娠前と妊娠後の感染の確率を推定できる.たとえば,妊娠前に合計100回レバ刺しを食し,妊娠後は1回であれば100対1となる.
職業では,生肉や土,猫を扱うことがリスクであり,家族歴では,両親が抗体陽性であれば,実家での生活中に感染した可能性が高くリスクは低下するが,夫が陽性であれば,結婚後に感染した可能性が高くなり妊娠中の初感染の可能性も生じてくる.頸部リンパ節腫脹では,内科で診断されたり,外科で切除術を受けた症例もあり,感染時期を推定できることがあり,重要である.妊娠前にトキソプラズマ抗体が陽性であれば,リスクはなくなる.海外渡航歴では,ヨーロッパ・南米・アフリカがハイリスクであり,妊娠前にこれらの地域に長期に滞在していれば,先天感染のリスクは低下する.生活地域では,これらは馬刺摂取歴に一致する地域である.妊娠前に長年生活していればリスクは低下するが,妊娠後初めて生活し出せば,リスクは上昇すると推定される.ペット飼育歴も妊娠前であればリスクは低く,妊娠後初めてであればリスクは上昇する.嗜好では,馬刺,牛刺し,レバ刺し,鳥刺し,生ハム,サラミソーセージ,レアステーキ,その他(熊,鹿,山羊,猪,クジラなど)がリスクとなる.土埃などからの経粘膜感染の原因として,土いじり,井戸水の摂取,水洗いの不十分な野菜・果物の摂取,ネコの飼育などもリスクである.
トキソプラズマ症ハイリスク妊婦の管理法
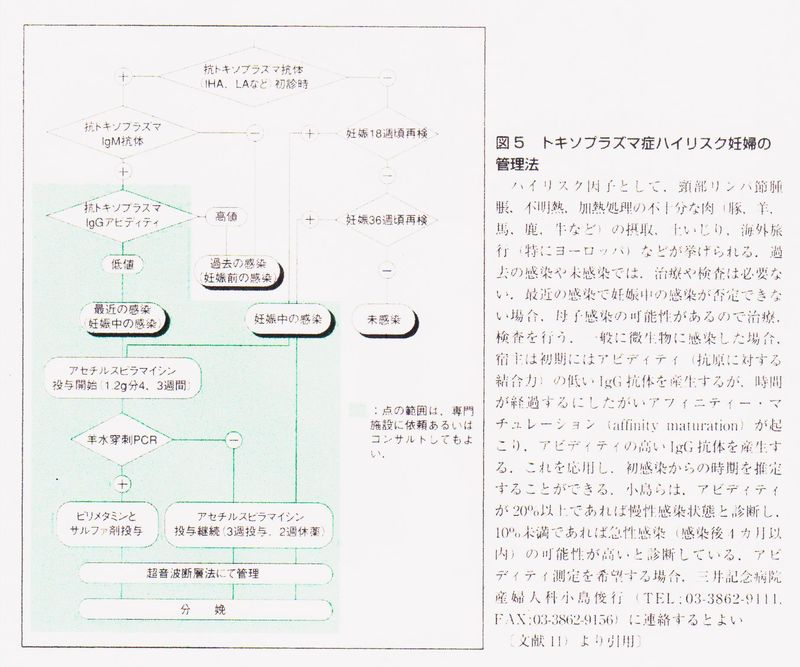
われわれの行っている妊婦のトキソプラズマ感染の管理法を図5に示した.11)
妊婦の感染時期とトキソプラズマlgG抗体の
アビディテイ
一般に微生物に感染した場合,宿主は初期には抗原に対する結合力(アビディティ)の低いIgG抗体を産生するが,時間が経過するにしたがいaffinity matUratiOnが起こり,アビディティの高いIgG抗体を産生する.これを応用し,初感染からの時期を推定することができる.図6にアビディティの測定原理を示し,図7にアビディティの感染後の推移を示した.表4にアビディティの解釈を示した.図8にトキソプラズマ急性感染妊婦の抗体値の推移の実際を示した.
これらにより,トキソプラズマIgM抗体陽性妊婦のうち,約85%は妊娠前の初感染と判定し,先天感染の可能性はほとんどないと診断し,無治療で分娩し,現在まで先天感染例を生じていない.

トキソプラズマ抗体の解釈
表5にトキソプラズマ抗体の解釈を示した.表6,表7にわれわれの症例からトキソプラズマ抗体判定のポイントを示した13).

母体治療
スピラマイシン,アセチルスピラマイシン,ピリメサミン,サルファ剤の特徴を表8~12に示した.母体が妊娠中の初感染が疑われる場合の,治療薬を表13に示した.これらを分娩まで服用することで,重症の先天感染発症の確率を非服用群に比べ14%にまで減少させると報告されている14)(表14).アセチルスピラマイシンは,1,200mg分4で21日間投与し,14日間休薬することを1クールとし,分娩まで継続する.200mg錠の場合には,朝1錠,昼2錠,夕1錠,就寝前2錠としている.羊水中にトキソプラズマのゲノムが検出できなければ,胎内感染は未だ成立していないと判断し,アセチルスピラマシンの投与を続行する.羊水中にトキソプラズマのゲノムが検出された場合,ファンシダール(SP錠;1錠中スルファドキシン500mg,ピリメタミン25 mg)に薬剤を変更し,超音波断層法を用い,胎児の脳室拡大,頭蓋内石灰化,肝腫大,腹水,胎盤の肥厚,羊水過多などの出現に注意しながら,管理を行う.ピリメタミンは動物での催奇性が報告されているので,妊婦には16週以前には投与しない.サルファ薬はアルブミンとの結合に際しビリルビンと競合するので,新生児に対する核黄疸の副作用があるため妊娠28週以降は禁忌とされている.したがって,ハイリスク群には,16週から27週までは,ファンシダール3週間とアセチルスピラマイシン3週間を交互に投与し,28週以降はアジスロマイシン3週間とアセチルスピラマイシン3週間を交互に分娩まで投与している.

母子感染率
妊婦のトキソプラズマ抗体が陽転した妊娠週数における母子感染率を図9に示した.妊娠8週で2~3%と低値で,97~98%は胎内感染しないことを示している.しかしこの冊数では胎内感染した2~3%の約半数は重症である.
出生児の管理

 出生児の管理を表15に示した.ローリスク群では,検査法をかなり省略したが,現在まで先天感染例は出生していない.先天性トキソプラズマ症の定義を表16に,出生時の先天性トキソプラズマ症の診断を表17に示した.非感染例でトキソプラズマIgG抗体の電動血/母体血比は1.48±0.48で膀帯血が高く,3未満であれば問題ない.先天性トキソプラズマ症の除外診断を表18に示した.
出生児の管理を表15に示した.ローリスク群では,検査法をかなり省略したが,現在まで先天感染例は出生していない.先天性トキソプラズマ症の定義を表16に,出生時の先天性トキソプラズマ症の診断を表17に示した.非感染例でトキソプラズマIgG抗体の電動血/母体血比は1.48±0.48で膀帯血が高く,3未満であれば問題ない.先天性トキソプラズマ症の除外診断を表18に示した.
以上,トキソプラズマ合併妊婦とその出生児の管理について概説した.
最後に,貴重な症例をご紹介頂いた全国の日本産婦人科医会,日本産科婦人科学会の会員の皆様に感謝致します.
■文献
1)J.S. Rem血gton, et aL:Infectious Diseases of the Fetus & Newborn lnfant 4th ed. Philadelphia:W.B. Saunders Company:140-267, 1995,
2) Zuber, P., and Jacquier, P. Epidemiologie de la toxoplasmose:situation au niveau mondial. Schweiz. Med. Wochenschr 125 (Suppl. 65) : 19S 22S, 1995.
3)小島俊行,Jack S, Remington,佐伯えみ,千野正子,渡部正臣,鈴木三郎,川名 尚:妊婦における抗トキソプラズマlgG,IgM抗体保有率とその測定法について.日本新生児学会誌34;420, 1998
4)野田俊一,野田 彬,柚木康彰,小島俊行,川名 尚,宮田和典,望月 學,池田智明,池ノ上克.南九州における妊婦のトキソプラズマスクリーニング.感染症学雑誌,74:192-193,2000.
5)Lebech M, et al.:Feasibility of neonatal screening for toxoplasma infection in the absence of prenatal treatment. Danish Congenital Toxoplasmosis Study Group. Lancet 353:18341837, 1999.
6)大内広子 妊婦のトキソプラズマ症について.日本医事新報,2595,129,1974.
7)Bowie, W. R, Kng, A S., Werker, D. H., lsaac Renton, J. L., Bell, A, Eng, S, B., and Marion, S. A. Outbreak of Toxoplasmosis Associated with Municipal Drinking Water. Lancet 350;173-177,1997.
8)小島俊行,野田俊一,佐藤俊則,野田 彬,池ノ上克.川名尚.堤治:トキソプラズマの母子感染の診断・予防に関する研究.周産期学シンポジウムNo.18メジカルビュー社,東京, 919, 2000.
9)小島俊行,吉田良一,吉田智子,堤 治,武谷雄二:胎児・新生児医療一’02年のトピックス妊婦のトキソプラズマIgM抗体陽性と出生児への感染.産婦の世界55;73-83,2003.
10)Cook AJC, et al.:Sources of toxoplasma infection in pregnant women:European multicentre case-control study. BMJ 321 : 142-147, 2000.
11)日本産婦人科医会研修委員会編:トキソプラズマ.研修ノートNo.66新生児のプライマリケア.日本産婦人科医会,4546,2002.
12)小島俊行:クリニカルカンファレンス 7.周産期医療と児の中長期予後 1)母子感染.日本国科婦人科学会雑誌53:N285-N290,2001.
13)小島俊行:トキソプラズマ抗体検査値のみかた,中外医学社(東京):622-627,2006.
14) Foulon W, et al.:Treatment of toxoplasmosis during pregnancy:a multicenter study of impact on fetal transmission and children’s sequelae at age1 year. American Journal of Obstetrics & Gynecology 180:410015, 1999.
15)Montoya JG, liesenfeld O:Toxoplasmosis. Lancet 1420;364 (9434) : 579, 2004.
16)小島俊行,安田 孝.中田真木,柿木成子,北條 智,塚崎雄大,濱崎かほり,花岡正智,粟田面里子,前田大地,崎川牧子,高屋 茜:周産期感染症ハンドブックートキソプラズマ.産婦の実際55:519・530,2006.
最近のコメント