(関連目次)→医療事故安全調査委員会 各学会の反応
(投稿:by 僻地の産科医)
Aiと剖検が独立した社会システムを
千葉県がんセンター画像診断部
高野英行
日経メディカルオンライン 2009.3.13
(1)http://medical.nikkeibp.co.jp/leaf/mem/pub/opinion/orgnl/200903/509804.html
(2)http://medical.nikkeibp.co.jp/leaf/mem/pub/opinion/orgnl/200903/509804_2.html
(3)http://medical.nikkeibp.co.jp/leaf/mem/pub/opinion/orgnl/200903/509804_3.html
(4)http://medical.nikkeibp.co.jp/leaf/mem/pub/opinion/orgnl/200903/509804_4.html
CTの導入以後の放射線診断の進歩は目を見張るものがある。私が放射線科医となった24年前のCTといえば、一呼吸ごとに、1cmスライスを数枚撮影するのが精一杯、MRIは数十分かけて数スライスが精一杯であった。しかし、現在のCTやMRIは、1mm未満の精度で3次元画像が容易に作れるレベルにまで達し、その像は、あたかも目の前にいる患者さんを解剖しているような錯覚を覚えるほど緻密で、病理標本に匹敵する画像が撮影できる。このAiを病理画像の代わりに普及させようと考え、活動する放射線科医、病理医、法医学者が増加していることは、合理的なことである。
しかしながら、Aiの利用法に対するポリシーや思惑の違いから、その運用に関しての齟齬が生じており、不透明な状況である。私が経験したことを通じて、一放射線医の立場から放射線科医の役割について述べてみたい。
骨の病変は放射線が有利、特に虐待では
私は、10年以上前、小児放射線医として米国で臨床を行っていた。ある朝のカンファレンスの後、上司のドクター・スミスが言った。「これから裁判所に行って証言してこなければいけないので…-」。
当時の私には、放射線科医と裁判所の関係が結びつかず、「なんで、裁判所なんかに?」と聞いてしまった。彼は、いくつかのフィルムをシャーカステンに掛けながら、「小児虐待(Battered child)の裁判で証言するんだ。ここに化骨のある古い骨折、ここに新しい斜めの骨折----、小児虐待の典型的な写真だろう」と言い放った。放射線科医が法廷で証言するのは当然というそぶりで。
小児放射線科医Frederic N. Silvermanは1953年American Journal of Roentogenology (AJR)に、”The roentgen manifestation of unrecognized skeletal trauma in infants. (乳児における気づかれない骨外傷のレントゲン所見) “で、原因不明であるが、特徴的なレントゲン所見の患者群を発表している。それは、1962年The Journal of the American Medical Association(JAMA)の”The Battered child syndrome”へと結実した。画像の読影に習熟した放射線科医が、事件性があると判断し、Battered child(小児虐待)という概念を導き出した歴史的な論文である。それに関わってきた放射線科医の鑑定が法廷で重要視されるのは、当然である。当時、日本で見た虐待は少なかったが、最近では、虐待が増えたのか、虐待が問題となり病院に来るようになったのか、多くの症例を見るようになってきている。
多くの医師にとって病理診断は絶対的なものかもしれないが、実は、顕微鏡下の病理診断は絶対的なものではない。医師ならば、学生時代の病理学の教科書を思い出してほしい。病理のプレパラートの写真と一緒に、骨のレントゲン写真が掲載されているのを一度は見たことがあるはずだ。骨の病理診断は、プレパラートのみでは難しい。一般病理医は、疲労骨折と骨肉腫を間違えることもある。私の恩師に当たる放射線科医が、整形外科の学会で、骨肉腫として病理診断、治療された症例として提示された術前レントゲン画像が疲労骨折の典型例だったという話をしてくれたことがある。恩師は、周囲の整形外科医もみな同意してくれたという逸話を話しながら、病理診断を鵜呑みにせず放射線診断を行うことの重要性を教えてくれた。
骨折の診断に最も適している方法は、病理検査ではなく、レントゲン写真や薄いスライスCTである。一般の解剖では、骨の全身検索は行われず、行われても、骨膜の治った陳旧性の骨折を見つけるには、全身の骨の骨膜を剥さねばならない。しかも、骨のプレパラートを作るために、カルシウムを脱灰するなどの手間と時間がかかり、全身を網羅的に検索することは不可能である。つまり検索しなかった骨に病変がないことを証明する方法がないのである。Aiにおいては、全身検索したことが容易に証明できる。
先日のAi学会において、致死性四肢短縮症(軟骨形成の異常)の一剖検例ということで、レントゲン写真で示された画像は、肋骨の短縮がなく、軟骨性の疾患は否定的な像であった(骨形成不全症により大腿骨の曲がりと短縮が起きたと考えられる)。しかし、大腿部の剖検では、明らかな間違いが気付かれなかった。そのため、会場でその間違いを指摘された。骨を読める放射線科医が読んでいれば、間違えようのない症例であった。放射線診断による全身像としてのとらえ方の重要性が認識された一例であった。
亀田ティオリン訴訟のトンデモ鑑定の原因は?
さて、日本では、放射線科医には裁判は関係ないだろうと思っていたが、亀田総合病院からの鑑定依頼が来た。いわゆる亀田テオフィリン訴訟である(詳細はロハスメディカルブログ)。その時に争点になったのが、中心静脈カテーテルの位置であった。
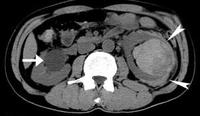 事件当時のマルチスライス・ヘリカルCTは、画質を犠牲にして早く撮影したため、前の世代のCTと比べると風車状に外側へ膨らむというアーチファクトがあった。それを補正したが、補正がかかるのは臓器などの軟部組織についてだけであり、高い濃度のカテでは実際の位置より外側に見えてしまうことがある(図1)。
事件当時のマルチスライス・ヘリカルCTは、画質を犠牲にして早く撮影したため、前の世代のCTと比べると風車状に外側へ膨らむというアーチファクトがあった。それを補正したが、補正がかかるのは臓器などの軟部組織についてだけであり、高い濃度のカテでは実際の位置より外側に見えてしまうことがある(図1)。
図1 アーチファクトによるカテーテル位置の誤認
左腕頭静脈(矢印)内の中心静脈内カテーテルは、外に飛び出して見える(矢頭)が、このカテーテルは挿入時に静脈内にあることが確認されており、トラブルなく使用されている。
このことを認識せずに、中心静脈カテの位置が、外側にあるように見えるので、これが静脈外に出て、動脈を傷つけたとの原告推薦鑑定者からトンデモ鑑定が出され、裁判では採用されてしまった。院内の解剖ではカテの入っている静脈の破れなし、死の直前CTでも、この透析用中心静脈カテから入れた多量の点滴(数リットル)が漏れていないことは明らかであるのに。
亀田テオフィリン訴訟において、院内解剖では、血管損傷がないという所見は裁判では採用されず、原告側のCTの読影所見が採用され、最高裁で確定した。カテーテル事故を疑った場合の院内解剖は証拠能力がないということが司法的には確定してしまったわけである。司法の場では今後この最高裁判決に基づき弁論が進められるのは明らかである。この判決は非常に重い意味を持っており、いわゆる医療事故調(医療安全調査委員会)の論議の際、必ず考慮されなければならないと思われる。
この訴訟においては、死後に大腿からの中心静脈カテから造影剤を注入してレントゲンやCTが撮影されていれば、後から客観的にカテが静脈を貫いていないということが証明できたはずである。医療事故が疑われた症例における客観的な記録保持方法としては、自院における解剖よりもAiの方が客観的であるということになるかもしれない。
Aiを理想的に行うには、統一したプロトコールでの撮影が必要である。それらによって得られた画像を、複数の他院の放射線科医により判定することにより、客観的に評価が可能であろう。そうでないなら、裁判で負けないためには、救急救命でカテーテルを入れて亡くなった患者すべてに司法解剖を行わなければならないことになる。ところが、司法解剖では、その開示が非常に遅かったり、非開示になることもあるため、遺族の不信を買い、逆に民事訴訟を増やす可能性が危惧される。
裁判員制度が始まり、一般の裁判員に状況を説明する手段として、Aiの有用性はさらに認識されることになるだろう。
コストパフォーマンスならAiは解剖を上回る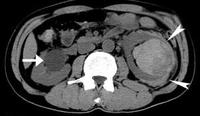
ところで、AiのCTで出血が見えるかどうかの議論があるが、出血してある程度の間(生体での反応と違うことにより期間は断定できないが、数日間)は、高信号に見えるはずである(図2)。
。
図2 単純腹部CTでの嚢胞(水)と血腫の違い
右腎には傍腎盂嚢胞があり、左は血尿で発症した腎出血である。造影剤を使用していないが、腎盂側と腎周囲に高信号があり、血腫であることが分かる。カテーテルにて、腎動脈をコイル塞栓し、軽快した。
被爆を減らしたスクリーニング用のCTであったり、線量調整などが適切でない機器であったり、表示方法が適切でなければ、腹部の出血の濃度差が見えない可能性はあります。使用する機械の特性や読影法に対する熟知が必要である(図3)。
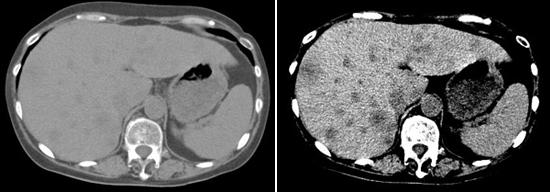
図3 表示条件の違いによる認識度の違い。(肝転移の描出)
2つの写真は同じCTである。左の写真は、通常の腹部単純CTの表示条件であるが、右の写真の肝臓に絞った濃度差を用いることにより、肝臓の腫瘤(転移)の認識能が高まる。読影には、CTの熟知が重要である。
また、時間が経ち、血腫の変性が進んだ慢性血腫などの場合は、CTでは、液体であることは分かるが、血腫由来であるか分からないことはあり得る。もちろん剖検により初めて分かる可能性もある。ただし、MRIは、古い出血の描出に優れている。
造影死後CTが可能であれば、CTによる死因究明率は大きく向上するはずだ。先日のAi学会では、国立病院機構東京医療センターから、死亡判定後に心マッサージを行いながら造影CTを行うことにより、動脈の破裂を診断できたとの報告があった。今後の研究により、冠動脈閉塞や肺塞栓などの血管性病変の診断ができる可能性がある。
コストパフォーマンスの点から、Aiと剖検の比較してみたい。
解剖すれば約8割の症例で死因が確定できるのに対し、死後CTによる死因究明率は約3割(造影CT, MRIでは5割以上と思われる)といわれている(日経メディカル オンライン「海堂×岩瀬●死後画像をめぐるトークバトル」)。一見Aiの有用性が低いように思われるが、現実の場での施行率とコストを考えるとその状況は一変する。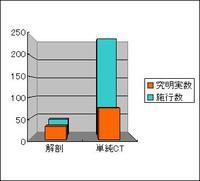 1000万円で可能な解剖数(約25万円、日本病理学会、日本法医学会)は施行40人。よって死因究明できるのは32人。死後CT(新患CTプラス付帯料金の医療保険の倍と仮定して約4万円と想定)ならば施行250人で、75人の死因が究明できる(図4)。同じコストを国民が払った場合の死因究明数は、CTの方が倍以上多いという結果になる。また、両者に血液による薬物検査や目視のコストを加味しても、この結果は大きく変わらない。
1000万円で可能な解剖数(約25万円、日本病理学会、日本法医学会)は施行40人。よって死因究明できるのは32人。死後CT(新患CTプラス付帯料金の医療保険の倍と仮定して約4万円と想定)ならば施行250人で、75人の死因が究明できる(図4)。同じコストを国民が払った場合の死因究明数は、CTの方が倍以上多いという結果になる。また、両者に血液による薬物検査や目視のコストを加味しても、この結果は大きく変わらない。
図4 同じコスト(1000万円)をかけた場合の死因究明実数の予想値単純CTの究明率は低いが、低コストで行えるため、死因究明される実数は、はるかに多い。
日本での解剖の施行率が3%とすると、死後単純CTの施行率が9%以上になれば、死因究明実数でも優位に立つ。Aiでは、死体の損壊を恐れる遺族への説得も容易であり、施行数の増加は容易であり、達成可能な数字である。造影CTやMRIのコストが6万円であれば、単純CTよりも優位である。
Aiだけで十分と考える放射線科医はいないが、独立性が重要
日本放射線科専門医会はAiワーキンググループを設け、制度の枠組みや撮影プロトコルなどの提案を作成中である。Aiの歴史は浅いが、院内解剖が司法では無視されるのであれば、客観的な情報であるAiの存在は重くなる。精度を上げるために剖検と切り離すべきではないという意見もあるが、過去の放射線診断の知識を集めれば、単独で運用できる部分もあると考えている。
例えば、CTで脳幹部出血が明らかな症例に関して、死因究明のための解剖が必要なのだろうか。また、救命救急の場に救急車で運ばれてきた心肺停止状態の患者(死者)の画像診断を行った際、その後、解剖が行われなければその画像診断は無意味になってしまうのだろうか。
Aiは解剖とは独立して存在することにより、その客観性がより保たれる。なぜなら、全身をくまなく検索したことが明瞭に分かるし、第三者を含めた検討が可能であるからである。ワーキンググループではAiのデータを集積し、利害のない複数の第三者による鑑定を可能にするシステムを提案する予定である。そのためには、Aiに対して、医療保険や剖検とは別枠の予算が必要だということも強調しておきたい。
もっとも、Aiだけで全てが終わると考えている放射線科医は一人もいない。Aiによる画像の診断能力は、病理解剖と比較検討することにより向上する。一方、Aiにより低侵襲に病変部位のみを取り出し、病理診断をすることは、病理診断の効率化につながり、死因究明率を向上させる手段にもなり得る。また、事件性が明らかな場合には司法解剖も必須である。
死因究明において、ネガティブデータも客観的に残し、評価する必要性があるとすると、Aiと解剖がシステムとして独立しながらも、両者を有機的に活用する社会的なシステム作りが必要と考える。
たかの ひでゆき
○1986年千葉大学医学部卒。
琉球大、沖縄県立中部病院、埼玉県立小児医療センター、
千葉大、米国アイオワ大学を経て2001年より現職。

コメント