(関連目次)→性感染症と中絶について考える 妊婦さんと感染症
(投稿:by 僻地の産科医)
今日から大阪でHIV学会ですo(^-^)o ..。*♡
本当はとってもいきたいのですが、ちょっと日程的に無理そうです。
 ちなみに母子感染のは木曜日13時より。
ちなみに母子感染のは木曜日13時より。
興味があって抜けられそうな方、せっかくですから足を運んでみてください!
HIV感染症治療の最前線と課題
独立行政法人国立病院機構大阪医療センター
HIV/AIDS先端医療開発センター
白阪 琢磨
(日本医事新報 N0.4401(2008年8月30日)p56-62)
【要 旨】
1996年頃に登場した多剤併用療法によってHIV感染症は慢性疾患になった。薬剤開発の進歩で服薬は以前より容易となったが、服薬アドヒアランスが重要である点は変わらない。本稿ではHIV感染症治療の現状と課題につき述べる。
はじめに
医学の進歩と世界保健機関(WHO)など関連機関の努力によって感染症対策は目覚ましく進歩した。ワクチンによる天然痘の撲滅宣言や最近のSARS終焉宣言などを例に挙げることができる。日常診療の現場でも抗菌薬の進歩によって、多くの細菌性感染症は治癒できる。しかし、今でも世界は感染症に苦しんでいる。WHOが結核、マラリアとともに世界の三大感染症の一つにエイズを位置づけた。本稿では、HIV感染症に対する治療薬開発の現状と今後の課題につき述べる。
AIDS、HIVの発見からHAART登場まで
1981年に、米国で原因不明の免疫不全症が世界で初めて報された。この疾患は、後に後天性免疫不全症候群(acquired immunodeficiency syndrome ;AIDS)と命名され、1983年に病原体としてヒト免疫不全ウイルス(human immunodeficiency virus ;HIV)が同定された。満屋裕明博士らが米国で開発した世界最初の抗HIV薬ジドブジン(AZT)が1987年、米国FDA(食品医薬品局)によって承認され、それ以後、薬剤開発が格段に進んだ。1995年暮れには、世界初のHIVプロテアーゼ阻害薬(protease inhibitor ;PI)が米国FDAによって承認された。この頃、HIV-Iの血中ウイルス量(viral load ;VL)を測定する技術も開発され、抗HIV薬の臨床効果を血中HIV-IのVLの変化で評価できるようになった。
HIV感染症の治療効果のエンドポイントは本来、AIDS発症率あるいは死亡率であり、治療効果はこれらの指標をどれだけ低下できるかで評価されるので、VLや眼中のCD4陽性Tリンパ球数(以下、CD4値)はサロゲートマーカー(surrogate marker)と呼ばれていた。しかし、これらの指標は観察期間が比較的短期間でよく、その後の臨床試験成績から、抗HIV薬の治療効果はVLと血中CD4値で十分評価できることが分かった。
VLの減少で比較すると、PIの効果は既存の核酸系逆転写酵素阻害薬(nucleoside reverse transcriptase inhibitor ; NRTI)を大きく凌ぐものであった。PI1剤とNRTI2剤を組み合わせた3剤による多剤併用療法により、VLは数カ月で測定検出限界値(当時は400コピー/ml)未満に抑えられ、血中CD4値も徐々に上昇することが分かった。この3剤併用療法は、その強力な効果からhighly active anti-retroviral therapy(HAART)と呼ばれた。やがて、死に瀕したAIDS発病者がHAARTによって社会復帰したとの報告が驚きを持って迎えられた。その後の臨床経験の蓄積から、HAARTによってサロゲートマーカーの改善のみならず、HIV感染症の予後は改善できることが明らかとなり(図1)、HIV感染症も慢性疾患と認識できる時代が到来した。
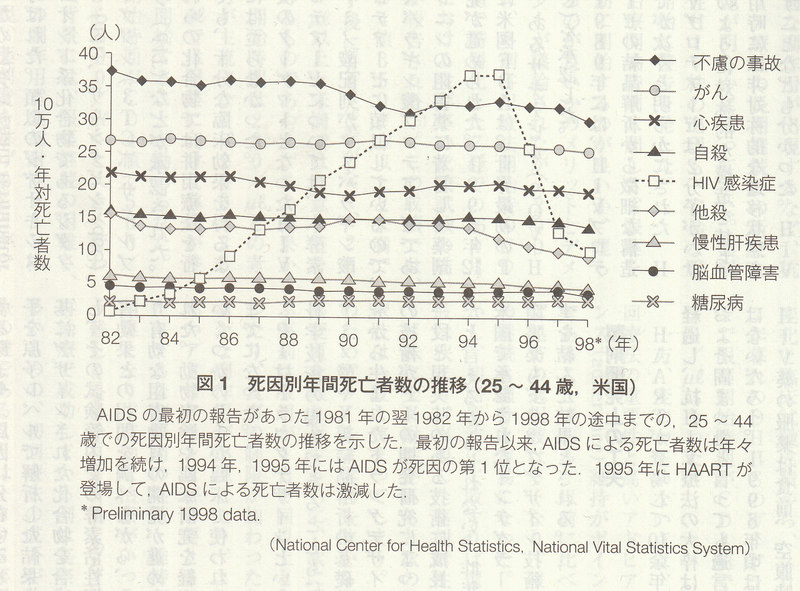
この治療の飛躍的な進歩を踏まえて、IAS-USA(International AIDS Society‐USA)の専門家や米国保健福祉省(DHHS)が中心となって、HIV感染症治療のガイドラインをそれぞれ作成した。我が国でもHIV感染症治療研究会や厚生省(当時)の研究班が治療のガイドラインを作成した。続いてネビラピン(NVP)、エファビレンツ(EFV)という非核酸系逆転写酵素阻害薬(non‐nucleoside reverse transcriptase inhibitor ; NNRTI)が登場した。特にEFVは、PIに勝るとも劣らない抗ウイルス効果を示した。抗ウイルス効果はPIあるいはNNRTIのほうがNRTIよりも強いので、最近ではPIあるいはNNRTIをキードラッグ、NRTIをバックボーンと呼ぶ。NRTIを2剤組み合わせる理由は他書を参照されたい。
ドラッグデザイン
AZTは細胞内で代謝され、AZT三リン酸化物となって逆転写酵素活性を阻害する。AZTの化学構造上の特徴は、チミジンのヌクレオシドの糖の部分の.3の水酸基がアジド基に、2'の水酸基が水素に置換されている点である。AZT三リン酸化物を取り込んだ逆転写酵素はDNA鎖を伸張できないため,DNA chain terminatorと呼ばれた。類似のジデオキシヌクレオシド系化合物であるジダノシン(ddI)、ザルシタビン(ddC)、ラミブジン(3TC)、サニルブジン(d4T)などが承認された。これらの化合物では併用療法を行っても、十分な臨床効果を得るまでには至らなかった。
次のターゲットとなったHIVプロテアーゼについては、本酵素のアミノ酸配列がアスパラギン酸プロテアーゼに類似しているので、アスパラギン酸プロテアーゼであるレニンの阻害薬に着目して薬剤開発が進められた。1995年12月に米国FDAは、世界最初のPIであるサキナビル(SQV-HGC)を承認した。
1989年には、HIVプロテアーゼの結晶解析から微細な構造までが次々と明らかにされた。HIVプロテアーゼは2分子がハサミのように対称的な構造を持ち、作用時には非対称的な遷移状態を示すことなども分かった。HIVプロテアーゼの構造解析から、活性中心部位を取り囲む近傍の空間を構成するアミノ酸の側鎖を構成する原子や、周囲に分布する水分子を原子レベルで解析した結果を基にデザインされた化合物を合成し、その試験管内での酵素活性阻害効果との相関を調べながら、より有効な阻害物質の開発が進められた。動物実験や臨床研究を経て、いくつかのPIが臨床で使われるまでになった。
PIはドラッグデザインという科学技術の賜物であるとともに、アミノ酸やX線結晶解析の基礎研究から生まれたドラッグデザインの技術がPIの開発研究によって一段と現実昧のある技術に成長したと言えるかもしれない。昨年、米国で承認されたインテグラーゼ阻害薬もドラッグデザイン技術が実を結んだ結果とされる。
製剤開発上の工夫
HAARTが登場して10余年が経過し、抗HIV療法の大枠はおおよそ固まったと言っても過言ではないだろう。1996年頃は抗HIV薬の服薬は食前、空腹時、食後であったので1日に20錠以上を6回かそれ以上に分け、さらに副作用出現の予防のために1日に1・5L以上の余分な飲水が必要とされるなど、服用自体が困難を極める状況にあった。HIV感染者の生存を保証したHAARTであったが、服薬がきわめて困難であったために、仕事を辞め療養に専念した者や、遂に服薬を諦めた者もあった。HIVの感染細胞の寿命に関する研究から、服薬期間は60~70年が必要とされた。
AIDS発病を延ばすためには、いったん開始した服薬をほぼ生涯にわたって継続する必要があるので、薬剤開発の新たな目標として服用が容易な製剤の開発へと進んだ。その結果、錠数を減らすために既存の抗HIV薬を組み合わせた合剤が開発され、剤型も小さくなり、食事の影響が少ない薬剤が登場してきた。現在は1日1回、3カプセルと1錠を服用すればよい組み合わせが可能となった。3種類の抗HIV薬、テノホビル(TDF)、エムトリシタビン(FTC)、EFVを1錠に凝縮した錠剤が海外で承認され、1日1回1錠が汎用されている。
PIは薬物代謝に関係するCYP450の活性を増強あるいは抑制するが、特にリトナビル(RTV)によるCYP3A4の阻害作用は非常に強い。そのため、CYP3A4で主に代謝されるPIでは、少量のRTVを併用することによってPIの代謝を大きく阻害できるので、錠数も減らすことができ、有効血中濃度を維持でき、さらに半減期の延長も得られる。これをRTVのブースター効果と呼び、ロピナビル(LPV)、アタザナビル(ATV)、ホスアンプレナビル(FPV)などではRTVカプセルを併用することによって、1日1回投与が実現された。
ガイドラインの変遷
多剤併用療法が登場して約10年間で、抗HIV療法の考え方には大きく変わった点と変わっていない点がある。大きく変わった点は治療の開始時期である。1996年当初は抗HIV療法の目覚ましい効果が注目され、“Hit HIV early and hard ”と言われ、CD4値が500/μ以下、VLが5000コピーノ・以上での開始が勧められた。しかし、実際に抗HIV療法を実施すると、短期服用での副作用に加えて長期服用でも深刻な副作用が出現するなど、抗HIV療法の長期継続での新たな課題が明らかになってきた。薬剤耐性HIV株の出現も、安易な服薬開始に警告を発した。
治療開始時期に関して、服薬を早期に開始するのが良いか、遅らせるのが良いかのメリットとデメリットが議論されたが、2001年に、多剤併用療法開始時のCD4値で階層化した7群での36カ月間における生存率の比較試験の結果が報告された印。この成績では、CD4値350/μl以上と未満では予後に大きな差がなく、200/μl以上と未満では有意な差を認めるものであった。この結果から、開始時期は200/μとの考え方が主流になり、200~350/μlでは服薬に向けた準備が整えば開始することが勧められた。
開始時期がCD4値で500/μlから200/μlへと大きく変わった背景には、服薬継続の困難さ、種々の副作用、薬剤耐性HIV株の出現、薬剤費を挙げることができる。その後、服薬が以前に比べ容易となり、服薬に伴う課題の多くがさらに克服された。これらの変化と臨床試験成績から、2007年暮れのDHHSのガイドラインで服薬開始時期がCD4値で350/μlになった。
一方、変わっていない点は、初回療法の重要性と高いアドヒアランス(乱回g回乙維持がポイントであることである。以前に比べれば処方の選択肢は多くなり、服薬の継続も随分と容易になった。しかし、初回療法に失敗すれば選択肢は狭まり、出現した薬剤耐性HIV株に交叉耐性があると次の選択肢は一段と狭まってしまう。そのため、ウイルス学的失敗から服薬変更を繰り返すうちに、次に選ぶ薬剤は服用が1日2回以上となったり、食事の制限が加わったり、新たな副作用が出現したり、より高いアドヒアランスが必要とされたりするなど服用の継続・維持が困難となり、有効な治療がいっそう難しくなってしまうであろう。再治療で成功している例は実際に多いものの、初回療法の成否が治療の鍵であることは1996年以来、変わっていない。
高い服薬率は多くの治療薬に求められ、医学では服用についてコンプライアンスという用語がある。抗HIV薬の服薬率は、95%以上でなければ良好な治療効果が得られないとの報告がある。医師の指示に従って服薬するという受け身的服薬行為では、このような高い服薬率の達成は困難であり、患者本人の意思で積極的に、主体的に服用する必要性が指摘され、その点を強調してアドヒアランスという用語が抗HIV療法の領域で使用される。
長期間継続して高いアドヒアランスを維持するためには、本人自身が服薬の必要性をよく理解し、自らが積極的に服薬することが重要であり、予期される主な副作用と対処法もある程度、事前に把握しておくのが望ましい。患者が有効な服薬を継続・維持するためには、患者自身の工夫と努力が重要であるが、次項のチーム医療の提供も有効である。
チーム医療の提供
 多剤併用療法の継続実施によってHIV感染症は確かに慢性疾患となったが、患者が高いアドヒアランスを維持するには多くの支援が必要であり、医療サイドからの支援が有効な場合も少なくない。患者は病気によって身体的だけではなく、精神・心理的、社会的、経済的な負担が生じることが多いが、HIV感染症の場合には感染が明らかとなることで身体以外の負担が大きく出現し、さらに以前から潜在していた各種問題が感染の判明を契機に顕在化して大きく患者の負担となることもある。
多剤併用療法の継続実施によってHIV感染症は確かに慢性疾患となったが、患者が高いアドヒアランスを維持するには多くの支援が必要であり、医療サイドからの支援が有効な場合も少なくない。患者は病気によって身体的だけではなく、精神・心理的、社会的、経済的な負担が生じることが多いが、HIV感染症の場合には感染が明らかとなることで身体以外の負担が大きく出現し、さらに以前から潜在していた各種問題が感染の判明を契機に顕在化して大きく患者の負担となることもある。
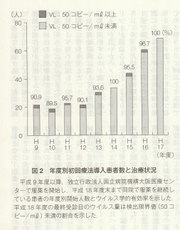
抗HIV療法におけるチーム医療の目的は、患者自身が服薬も含め自己管理をできるようになり、患者が健康を向上・維持できることにある。服薬という行為には阻害因子と促進因子があり、身体的・心理的・社会経済的要因があることが知られているので、服薬アドヒアランスの向ヒと維持には多方面からの総合的支援が必要である。そのため、患者の服薬に必要な支援をチームで提供することが重要となる。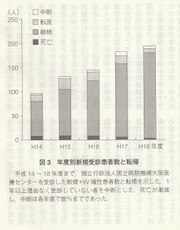 当院では早くからチーム医療の実施を心がけ、医師、看護師、薬剤師、臨床心理上、ソーシャルワーカーらからなるチームで取り組んできた。当院で抗HIV療法を開始し継続している患者における治療有効率(VL50コピー/ml未満を持続している患者の割合)を見ると、抗HIV薬が年ごとに異なっているためか開始年度により有効率が異なっているが約90%(89・5~100%)であった(図2)。また年度ごとの新規受診患者の中で受診中断例は数%にとどまった(図3)。これらはチーム医療の有効性を示すものと考える。
当院では早くからチーム医療の実施を心がけ、医師、看護師、薬剤師、臨床心理上、ソーシャルワーカーらからなるチームで取り組んできた。当院で抗HIV療法を開始し継続している患者における治療有効率(VL50コピー/ml未満を持続している患者の割合)を見ると、抗HIV薬が年ごとに異なっているためか開始年度により有効率が異なっているが約90%(89・5~100%)であった(図2)。また年度ごとの新規受診患者の中で受診中断例は数%にとどまった(図3)。これらはチーム医療の有効性を示すものと考える。
チーム医療の提供とは、患者に提供すべき医療を各スタッフが専門に応じて役割を分担し、患者と同じ目線に立って責任を持って行うことである。スタッフは専門的知識と技能、コミュニケーションスキルを持ち、自分の役割を認識し、責任を果たし、対患者のみならずスタッフ相互間においても良好なコミュニケーションを図ることが重要である。
治療の実際
抗HIV療法のガイドラインは毎年のように改訂されているが、最近の治療の実際をまとめた。
(1)開始時期
抗HIV療法を早期に開始する場合の長所と短所、治療を遅らせた場合の長所と短所を踏まえ、両者をよく検討して、最終的には患者本人とよく話をして、本人の納得を得て治療を開始する。前述の通り、CD4値が350/μl以下での開始が勧められ、CD4値がAIDSを発症しやすいとされる200/μlに近いほど、開始が強く勧められる。
治療開始の実際では、CD4値に加えて患者自身が治療への準備がどれだけできているか(readiness)が重要であり、CD4値の減少の速さ、VLを考慮に入れる必要がある。服薬準備ができていないのに開始してしまうと治療失敗に至るケースが少なくない。準備状況には患者自身が疾患を理解できており、多剤併用療法の必要性、抗HIV療法のメリット・デメリットの理解、心理的支援の必要性と具体的な支援の有無、社会あるいは経済的支援の状況、本人のライフスタイルに合った処方かなど、いくつかのチェックポイントが含まれる。
我が国では、HIV感染症は免疫機能障害という身体障害認定の対象であり、治療を要する患者では、申請によって多くが身体障害者手帳の取得と自立支援医療を受けることができる。健康保険の使用に不安を抱く例や身体障害認定等の申請に戸惑う例も多いので、治療開始前にソーシャルワーカーヘの相談を勧めるほうが良い。HIV感染を心理的に受け入れることができない例では服薬中断も見られるので、臨床心理士などのカウンセラーに相談するのが良いであろう。PIでは併用禁忌、注意薬が多いので、服薬している薬剤に注意が必要である。
(2)選択薬剤(表1)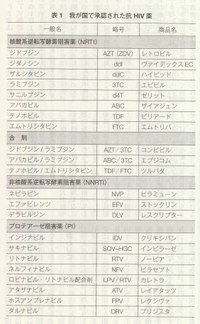 薬剤の好ましい組み合わせとして、キードラッグはNNRTIならEFV、PIならATV+RTV、FPV+RTV、DRV+RTV、LPV/RTVから選び、バックボーンとしてTVD(FTCとTDFの合剤)かEZC(3TCとABCの合剤)から選び、組み合わせる。これら以外にも多くの組み合わせが、代替えと位置づけられている。最近の推奨の基準には、治療効果に加えて服薬の容易さが含まれている。
薬剤の好ましい組み合わせとして、キードラッグはNNRTIならEFV、PIならATV+RTV、FPV+RTV、DRV+RTV、LPV/RTVから選び、バックボーンとしてTVD(FTCとTDFの合剤)かEZC(3TCとABCの合剤)から選び、組み合わせる。これら以外にも多くの組み合わせが、代替えと位置づけられている。最近の推奨の基準には、治療効果に加えて服薬の容易さが含まれている。
IAS-USAによれば、薬剤の選択に当たって治療前の薬剤耐性プロファイル、HBV肝炎の合併の有無、脂質代謝、糖代謝、冠疾患、肝機能、腎機能の異常の有無と程度、女性では妊娠や避妊薬の使用状況、常備薬などを聴取し、その内容を考慮することも重要とされている。EFVは催奇形性があるとされ、女性では妊娠初期あるいは妊娠の可能性のある場合には使用しない。欧米ではEFV、TDF、FTCという3剤の合剤(アトリプラごが承認されており、1日1回1錠の選択もある。
PIでは、前述のように少量のRTV併用によってATV、FPVの1日1回服用が可能となった。RTVカプセルは冷所保存が必要であるが、LPV/RTVという合剤(カレトラ)では室温保管が可能である。ただ、LPV/RTVでは他のPIよりも血清中性脂肪値の上昇やリポディストロフィーなどの副作用が出現することが多く、ATV、FPVなどの他のPIへ変更する場合もある。
アバカビル(ABC)の過敏症とHLA‐B※5701との関連や、EFVの血中濃度上昇とCYPの遺伝子多型との関係など、これらの遺伝子多型の事前診断によって治療の個別化が可能となるかもしれない。
NRTI併用の組み合わせでは、AZTと云『は同じチミジン系であり併用できないし、3TCとFTCも同じシチジン系であり併用しない。3TCとABCとの合剤(エプジコムごや、FTCとTDFの合剤(ツルバダごは、いずれも1日1回1錠の服用でよく、汎用されている。TDFは腎機能障害の既往例に投与すると腎機能障害が出現あるいは増悪することがあるので、TDF投与時は腎機能に注意し、増悪傾向があれば変更など対応が必要である。
(3)治療の目標と効果
治療の目標は、まず本人が服薬を規則正しく継続して実施することである。そうすれば、血中VLを測定検出感度(50コピー/ml)未満に抑え込め、その状態を長期に継続できればCD4値はやがて上昇してくる。血中のVLが測定検出感度未満であればHIVの増殖はかなり抑えられていると考えられるので、薬剤耐性変異株も出現しにくいと考えられる。言い換えれば、薬剤耐性変異株を出現させないためにもVLを抑え続けることが重要であり、治療目標はVLを測定検出感度未満に抑え続けることと言える。
CD4値の上昇の速度などの治療効果は、治療前のCD4値や年齢等によっても異なる。治療開始後もVLの低下が緩やかであり、24週後のVLが400コピー/ml以上の場合には効果不十分と判定される。もし、効果不十分の原因を十分に明らかにすることなく安易に服薬内容を変更すれば、同じ原因で再度失敗の可能性があり、選択肢を狭める結果になるので、その原因を十分に明らかにして対策を考えることが肝要である。
おわりに
HAARTが登場した1996年頃を機にHIV感染症のイメージは大きく変化した。HAART以前、HIV感染症は感染後5~10年でAIDSを発病し死に至る病であったが、HAART以後は医学的コントロールが可能な慢性疾患となった。しかし、現在でも治療薬はないので服薬を開始すると半永久的治療が原則である。HIV感染症が発展途上国で猛威を振るっていることを考えれば、服用方法は週に1回くらいで、数錠までが良く、副作用がほとんどなく、安価で、しかも有効な薬剤の開発が強く望まれていると思う。また、そのような薬剤が開発されれば、服薬の開始時期は現在より早くなる可能性もある。
HIV感染症に対する治療の最終目標は治癒であり、感染予防のワクチンの開発である。HIVは高変異性を特徴としており、ワクチン開発は困難を極めているとされている。HIVワクチンが実現するまで時間がかかるかもしれないが、HAARTで病状を安定させ健康を維持し続けるという戦略は勝算が十分にあると考える。HIV感染症の治療の分野では、医療の提供側も受給側も賢明に治療を選ぶ時代となった。

ぜんぜん知らないことばかりで、勉強になります。
本当はもっと知らなきゃいけないことなんだけど、なかなか手が回りません。
投稿情報: 山口(産婦人科) | 2008年11 月26日 (水) 12:06
そうなんです。
手が回らない。。。(;;)。
投稿情報: 僻地の産科医 | 2008年11 月26日 (水) 19:39
HIVについては恥ずかしながらまったく不勉強なんですが、日本に置ける感染症教育の第一人者:青木先生のblog見ていたらHIVの感染ルートの話の中で「どの地域でも男性の10~20人に1人は男性とセックスをするといわれており」とあって、ぎょええええ!!!と思ったしだいであります。
http://blog.goo.ne.jp/idconsult/e/07a1a58cdf74f596751b49e60f87252f
投稿情報: お弟子 | 2008年11 月30日 (日) 13:34